| Salicylzuur | ||||
|---|---|---|---|---|
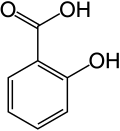
| Structuurformule en molecuulmodel | ||||
| ||||
Structuurformule van salicylzuur
| ||||
| Algemeen | ||||
| Molecuulformule | ||||
| IUPAC-naam | 2-hydroxybenzoëzuur | |||
| Molmassa | 138,12074 g/mol | |||
| SMILES | C1=CC=C(C(=C1)C(=O)O)O
| |||
| InChI | 1S/C7H6O3/c8-6-4-2-1-3-5(6)7(9)10/h1-4,8H,(H,9,10)
| |||
| CAS-nummer | 69-72-7 | |||
| EG-nummer | 200-712-3 | |||
| PubChem | 338 | |||
| Wikidata | Q193572 | |||
| Vergelijkbaar met | 4-hydroxybenzoëzuur en 3-hydroxybenzoëzuur | |||
| Waarschuwingen en veiligheidsmaatregelen | ||||
| ||||
| H-zinnen | H302 - H318 | |||
| EUH-zinnen | geen | |||
| P-zinnen | P280 - P305+P351+P338 | |||
| LD50 (ratten) | (oraal) 891 mg/kg | |||
| LD50 (konijnen) | (oraal) 1300 mg/kg | |||
| LD50 (muizen) | (oraal) 480 mg/kg | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vast | |||
| Kleur | kleurloos | |||
| Dichtheid | 1,44 g/cm³ | |||
| Smeltpunt | 158,3 °C | |||
| Kookpunt | 211 °C | |||
| Vlampunt | 157 °C | |||
| Oplosbaarheid in water | 2 bij 20°C g/L | |||
| Goed oplosbaar in | ethanol | |||
| Slecht oplosbaar in | water | |||
| Evenwichtsconstante(n) | pKz1 = 2.97 (carboxyl; 25 °C)[1] pKz2 = 13.82 (hydroxyl; 20 °C) | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Salicylzuur is een aromatisch carbonzuur en heeft als brutoformule C7H6O3. De zuivere stof komt voor als kleurloze en reukloze kristallen, die in water slecht oplosbaar zijn.
De stof is opgenomen in de WHO-modellijst van essentiële geneesmiddelen.
Voorkomen
Salicylzuur komt voor in onder andere wilgenbast, bepaalde soorten fruit, moerasspirea en sommige cactussen. Salicylzuur is een antioxidant die in planten en vruchten waarschijnlijk een functie vervult in de afweer tegen vraat en als conserveermiddel.
Synthese
De stof kan door middel van de Kolbe-Schmitt-reactie uit fenol worden bereid:
Structuur en eigenschappen
Salicylzuur heeft twee groepen, die kunnen worden geprotolyseerd. Dat zijn de fenolische hydroxylgroep met pKa = 12,38 en de carboxygroep met pKa = 2,97. Delokalisatie van de negatieve lading binnen de aromatische ring zorgt ervoor dat de zuursterkte aanmerkelijk groter is dan wat men zou verwachten van gewoon carbonzuur. Ondanks de zuursterkte is de stof nauwelijks oplosbaar in water. Zouten en esters van de stof worden salicylaten genoemd.
Toepassingen
Acetylsalicylzuur, bekend onder de merknaam Aspririne, is de azijnzure ester van salicylzuur. Salicylzuur werd voordat acetylsalicylzuur werd geproduceerd als koortsremmer gebruikt. Acetylsalicylzuur bleek behalve koortsremmend ook pijnstillend te werken.
Salicylzuur wordt in hoge concentraties tot 50% bij de behandeling van wratten gebruikt, omdat het met name de hoornlaag verweekt.[2] In lage concentraties van enkele procenten wordt het toegevoegd aan huidcrèmes om de penetratie van een geneesmiddel te bevorderen. Zo kan de geneeskrachtige stof gemakkelijker en sneller door de huid heen dringen. Op deze manier kan het ook helpen tegen acne.
Salicylzuur en verbindingen ervan werden als conserveermiddel in levensmiddelen gebruikt, maar dat is in de Europese Unie niet meer toegestaan. De esters met de carboxygroep van salicylzuur geuren erg aangenaam, een bekend voorbeeld is methylsalicylaat, dat naar de bloemen van de plant Gaultheria procumbens ruikt.
Verder kan het een precursor voor picrinezuur zijn: de carboxygroep kan door decarboxylering worden verwijderd.
Websites
 salicylzuur - International Chemical Safety Card
salicylzuur - International Chemical Safety Card- (en) Gegevens van salicylzuur in de GESTIS-stoffendatabank van het IFA
- ↑ DS Wishart, Y Djombou Feunang, AC Guo, EJ Lo, A Marcu, JR Grant, T Sajed, D Johnson, C Li, Z Sayeeda, N Assempour, I Iynkkaran, Y Liu, A Maciejewski, N Gale, A Wilson, L Chin, R Cummings, D Le, A Pon, C Knox en M Wilson. Salycylic acid, 2019. voor American Journal of Pharmacological Sciences 7, 1, blz 25-38
- ↑ NVDV. Wratten - Verruca.












