
Een mineraal is een in de natuur voorkomend element of anorganische verbinding met een omschreven chemische samenstelling en karakteristieke kristalstructuur.[1] Tot de mineralen behoren veel uiteenlopende vaste stoffen, variërend van zuivere elementen en eenvoudige zouten tot complexe silicaten die in duizenden vormen kunnen voorkomen. Veel mineralen zijn opgebouwd uit een vaste oplossing en hebben een variabele samenstelling. De wetenschap die de samenstelling en eigenschappen van mineralen bestudeert heet de mineralogie.
In de geologische betekenis worden mineralen meestal gezien als homogene stoffen die gevormd worden uit anorganische processen. Er bestaan echter ook biogene mineralen (zoals calciet), of mineralen die in scheikundige zin een organische verbinding zijn (zoals melliet). Silicaatmineralen vormen ongeveer 90% van de aardkorst.[2] Andere belangrijke groepen mineralen zijn bijvoorbeeld de sulfiden, oxiden, halogeniden, carbonaten, sulfaten en fosfaten.
De term 'mineraal' verwijst binnen de voedingsleer naar bepaalde anorganische micronutriënten die nodig zijn voor de groei en overleving van een organisme. Ionen van elementen als natrium (Na+), calcium (Ca2+) of chloor (Cl–) spelen een belangrijke rol in diverse fysiologische processen. Het onderscheid tussen de betekenissen is gradueel.
Geologie
[bewerken | brontekst bewerken]Mineralen zijn de belangrijkste bestanddelen van de vaste Aarde. Een mineraal kan worden gedefinieerd als een natuurlijk voorkomende, anorganische vaste stof met een welbepaalde chemische samenstelling (die enkel binnen bepaalde grenzen kan variëren) en een kristallijne structuur.[1] Omdat mineralen al sinds de prehistorie worden gebruikt is de wetenschap ervan, de mineralogie, een van de oudste menselijke kennisgebieden. Sommige mineralen zijn voor de mens van praktisch of economisch nut en worden als erts of delfstof uit de bodem ontgonnen.
Mineralen worden meestal beschreven en geclassificeerd aan de hand van hun chemische samenstelling. Hoewel sommige mineralen, zoals grafiet of diamant, slechts uit een enkel element bestaan (in dit geval koolstof), zijn de meeste mineralen ionaire verbindingen die uit een ordelijke rangschikking van kationen en anionen bestaan. Afhankelijk van de grootte en de lading van de ionen krijgt het mineraal een specifieke kristalstructuur. Pyriet (FeS2) is een mineraal dat een disulfide-ion als anion bevat. Gips (CaSO4·2H2O) bevat het samengestelde anion sulfaat en twee moleculen kristalwater.
Er zijn duizenden soorten mineralen beschreven, maar er zijn er slechts veertig die algemeen voorkomen in de aardkorst en de bestanddelen vormen van gesteenten. De belangrijkste groep van mineraal in de aardkorst is silicaat, een tetraëdische verbinding die in tal van variëteiten kan voorkomen, waaronder verschillende edelstenen. Hoewel mineralen buiten de silicaten relatief zeldzaam zijn, hebben ze vaak interessante toepassingen en zijn ze van groot economisch belang.[3]
-
Een bothryodaal kristal bestaande uit paarse bolstructuren van chalcedoon.
-
Kristallen van rhodochrosiet, een mineraal dat rijk is aan mangaan.
Scheikunde
[bewerken | brontekst bewerken]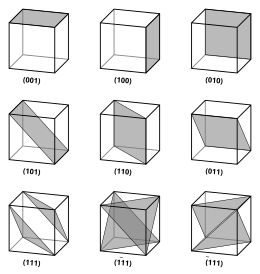
De abundantie en diversiteit van mineralen op aarde komt voort uit scheikundige condities en wetmatigheden. Met behulp van chemische benaderingen en technieken kunnen mineralen gekarakteriseerd en gegroepeerd worden. Kenmerkend voor mineralen is hun uiterst geordende atomaire structuur, waarbij de atomen in een regelmatig rooster gerangschikt zijn. Kristalchemici bestuderen de onderlinge verhoudingen van atomen, ionen of moleculen waaruit het kristalrooster is opgebouwd.[5]
De exacte chemische samenstelling van een mineraal is soms moeilijk vast te stellen, bijvoorbeeld door onzuiverheden. Sommige mineralen hebben daarnaast variabele verhoudingen van twee of meer chemische elementen die gelijkwaardige posities innemen in de kristalstructuur. De mineralenreeks plagioklaas bestaat bijvoorbeeld uit zes leden, van het natriumrijke albiet (NaAlSi3O8) tot het calciumrijke anorthiet (CaAl2Si2O8), met daartussen vier intermediaire variëteiten (in volgorde van natrium- naar calciumrijk): oligoklaas, andesien, labradoriet en bytowniet.[6]
Wanneer gesteente door subductie diep naar beneden wordt gesleept en daardoor wordt verwarmd en gedehydrateerd, raakt het getransformeerd, waardoor een grote verscheidenheid aan verschillende minerale assemblages ontstaat.
Voeding en fysiologie
[bewerken | brontekst bewerken]
Levende wezens hebben voor hun groei en overleving kleine hoeveelheden van bepaalde anorganische elementen nodig. Dergelijke micronutriënten worden in de voedingsleer mineralen genoemd.[7] Mineralen komen in kleine hoeveelheden voor in voedsel en water. De belangrijkste mineralen voor de mens zijn calcium, fosfor, kalium, natrium en magnesium. Andere elementen die een biochemische functie vervullen in het lichaam maar in veel lagere concentraties nodig zijn, zoals ijzer, zwavel, koper of zink, noemt men ook wel sporenelementen.[8]
De meeste sporenelementen die voor dieren essentieel zijn behoren tot de redoxactieve metalen, de overgangsmetalen in de vierde periode. Veel van deze elementen associëren zich binnen de cel als cofactor met enzymen. Sporenelementen die tot de niet-metalen behoren zijn seleen en jodium. Boor vervult enkele functies in planten, maar het komt ook in dierweefsels voor, zij het in uiterst lage concentraties. Zwaardere elementen, zoals arseen, cadmium, lood en kwik, hebben geen of een beperkte biologische functie en zijn over het algemeen giftig.[9]
Elektrolyten
[bewerken | brontekst bewerken]Anorganische verbindingen die in het lichaam in gedissocieerde vorm opgelost zijn, spelen vaak een belangrijke rol spelen in de fysiologie.[10] Dergelijke stoffen worden ook wel elektrolyten genoemd en splitsen in geladen ionen wanneer ze in water worden opgelost. Het mineraal natriumchloride (NaCl) splitst zich onder fysiologische omstandigheden bijvoorbeeld in natrium (Na+) en chloride (Cl–). In de extracellulaire vloeistof zijn natrium en chloride de belangrijkste elektrolyten. Kalium (K+) is vooral binnen de cel aanwezig, in het zogenaamde cytosol. Elektrolyten spelen een rol in verschillende lichaamsfuncties, bijvoorbeeld bij osmoregulatie, het zuur-base-evenwicht en de overdracht van elektrische impulsen in zenuwen en spieren.[11]
Zie ook
[bewerken | brontekst bewerken]Bronnen
- ↑ a b (en) Wenk H, Bulakh A. (2004). Minerals: Their Constitution and Origin. Cambridge University Press, p. 10. ISBN 978-0-521-52958-7.
- ↑ (en) Klein C, Hurlbut C. (1993). Manual of mineralogy, 21st. Wiley, New York, 440. ISBN 047157452X.
- ↑ (en) Tarbuck E, Lutgens F. (2013). Earth: An Introduction to Physical Geology, 11th ed. Prentice Hall. ISBN 978-0-321-81406-7.
- ↑ (en) Tilley, R. (2006). Crystals and Crystal Structures. John Wiley & Sons, "Latices, planes and directions". ISBN 978-0-470-02953-4.
- ↑ (en) Mukherjee S. (2011). Mineral Chemistry. In: Applied Mineralogy. Springer, Dordrecht. ISBN 978-94-007-1161-7.
- ↑ (en) Dyar M, Gunter M. (2008). Mineralogy and Optical Mineralogy. Mineralogical Society of America, Chantilly, VA, p. 586. ISBN 978-0-939950-81-2.
- ↑ Mineralen. Voedingscentrum. Geraadpleegd op 03-02-2024.
- ↑ Zoroddu MA, Aaseth J, Crisponi G, Medici S, Peana M, Nurchi VM (2019). The essential metals for humans: a brief overview. J. Inorg. Biochem. 195: 120–29. PMID 30939379. DOI: 10.1016/j.jinorgbio.2019.03.013.
- ↑ (en) Selinus O, Finkelman R, Centeno J. (2019). Encyclopedia of Environmental Health, 2nd. Elsevier, "Principles of Medical Geology", pp. 364-371. ISBN 978-0-444-52272-6.
- ↑ (en) Shrimanker I, Bhattarai S. (2024). StatPearls. StatPearls Publishing, "Electrolytes".
- ↑ (en) Lobo, D. N. (2004). Fluid, electrolytes and nutrition: physiological and clinical aspects. Proceedings of the Nutrition Society 6e (3): 453-466. DOI: 10.1079/PNS2004376.
Literatuur
- Burke, E.A.J. (1984). Mineralogie en mineralen. GEA: 90-91.
- (en) Bruce, C. (2015). Understanding Minerals & Crystals. Penguin Random House. ISBN 978-1-77584-334-4.
- (en) Selinus, O. (2013). Essentials of Medical Geology. Springer Science, "Chapter 8: Geological Impacts on Nutrition", pp. 179-194.











